人类多能干细胞(HPSCs)在再生医学领域有着广阔的应用前景,因为它们能产生体内的每一种细胞类型,并具有无限期繁殖的能力。然而,他们的潜能受到身体排斥任何“异基因”细胞或组织的倾向的阻碍,这意味着这些细胞来自于患者以外的供体。这种排斥是由于人体的免疫系统将这些细胞贴上“外来入侵者”的标签,并启动了一系列旨在抵御其认为是攻击的策略--这使得研究人员争先恐后地寻找绕过这种保护措施的方法。

今天《干细胞》杂志发表的一篇论文详细描述了可能提供答案的方法。作者报告中说,他们是如何从基因上排除了在HPSCs表面发现的一组关键蛋白,这些蛋白质是免疫排斥的目标,这样可以使它们在人体免疫系统中基本不可见。
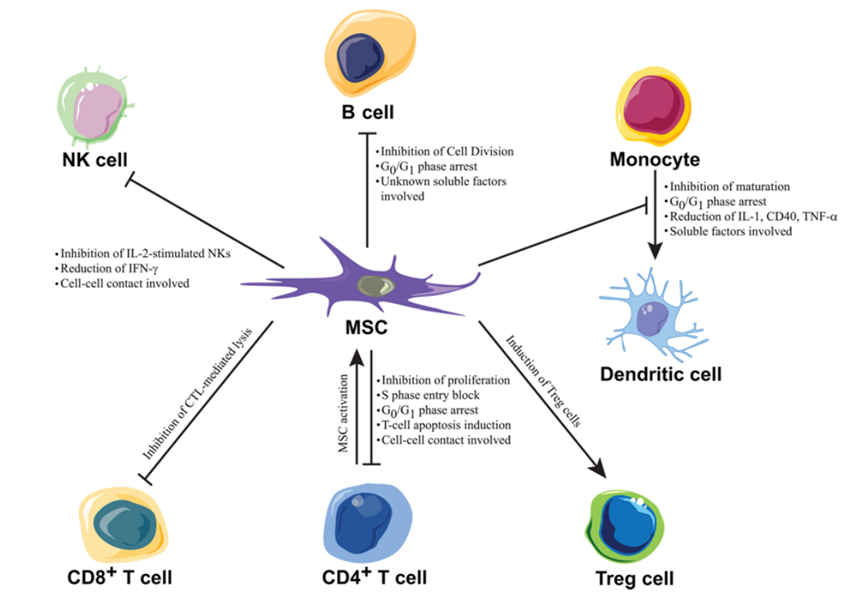
该多机构研究小组由同济大学医学院的科研团队领导的。作者称:“我们所做的是利用非经典的人类白细胞抗原(HLA)分子来构建低免疫原性HPSCs,这些分子编码同种异体排斥反应的主要靶点。我们的策略不仅改善了人体主要的免疫排斥武器--T细胞特别是CD8+TS,自然杀伤(NK)细胞和抗原提呈细胞--同时也减弱了细胞接触触发的细胞杀伤和同种异体环境的免疫原性。”
这项工作是因为他们知道HLA-G家族是胎盘中最显著表达的HLA-Ⅰ类分子之一,其作用是保护胎儿组织不受母亲免疫系统的影响。“这是哺乳动物免疫调节的一个显著例子,”作者解释道。因此,我们利用CRISPR/Cas9基因编辑技术,对β-2微球蛋白(β2m)敲除hPSCs,或在内源性β2M位点内进行HLA-G1双等位基因敲除。消除hPSCs表面表达,保护其免受CD8+T和NK细胞介导的细胞毒性。表面表达缺失还导致缺乏自我识别和异常的NK细胞激活。
EngineeredHumanPluripotentStemCells
《干细胞》杂志编辑JanNolta博士说,“这种将多功能干细胞衍生物从免疫系统中保护起来的方法在这个领域是一个‘改变游戏规则的人’。如果这一创新技术下一次被推广到临床试验中,这可能意味着这些细胞的受体将不需要免疫抑制。我们非常高兴地发表这一新的和可能改变范式的研究。”
另一位作者补充说:“据我们所知,这是第一次报告工程β2M-HLA-G5蛋白是可溶性的、可分泌的,并能有效地保护供体细胞免受免疫应答。这不仅提供了一种新的策略来生成低免疫原性的人类细胞供移植,而且还揭示了HLA-G在妊娠和器官移植期间免疫耐受中的作用。”
更多信息:STEMCELLS(2020).DOI:10.1002/





